一、热能和机械能的相互转换过程
1、工质与热源
工质是实现热能和机械能相互转化的媒介物质。热源是与工质进行热交换的物质系统。
从工质中吸取热能的物质系统,称为高温热源,简称“热源”;接受工质排除热能的物质系统,称为低温热源,简称“冷源”。环境大气可以看做为恒温热源,而如燃气轮机的高温排气看做变温热源。
2、热能和机械能的相互转换
热能动力装置的工作过程为:工质循环、自热源吸热,将其中一部分转化为机械能,并把余下部分传给低温热源;在制冷装置中,工质消耗外部机械功或其他形式的能量,使热能由低温热源向高温热源转移,所消耗的机械能也转换成热能一并排向高温热源。
二、热力系统
与外界没有物质交换,保持质量不变的系统,叫做闭口系;反之,与外界有物质交换的,叫做开口系,开口系强调物质可以交换,但是变化前后质量不一定会发生变化。两者之间区别仅仅在于物质交换。
与外界没有能量交换的系统,叫做绝热系;与外界无任何形式的质能交换叫做孤立系,此处的强调的是任何形式的能量,包括质量交换,其约束更强。
简单可压缩系由可压缩流体组成,与外界有交换体积变化功的有限物质系统。
三、工质的热力学状态及其基本状态参数
1、热力学状态和状态参数
热力学状态指某一瞬间系统所呈现的宏观物理状况。状态参数是描述物系所处平衡状态的宏观物理量。
2、状态参数的特性与分类
状态参数是宏观量,是大量粒子的统计平均效应,只有平衡态才有状态参数,系统有多个状态参数,例如:
状态参数是热力系统状态的单值函数。物理上,其与过程无关;数学上,其微量是全微分,闭合回路积分值为
状态参数可以分为强度量和广延量。强度量是与系统质量多少无关的参数,如
3、系统状态相同的充分必要条件
系统两个状态相同的充分必要条件为所有状态参数一一对应相等;简单可压缩两状态相同的充要条件为两个独立的状态参数对应相等。
4、温度和温标
温度是物体冷热程度的标志。测温的基础是热力学第零定律。
5、压力
绝对压力,也称真实压力,使用
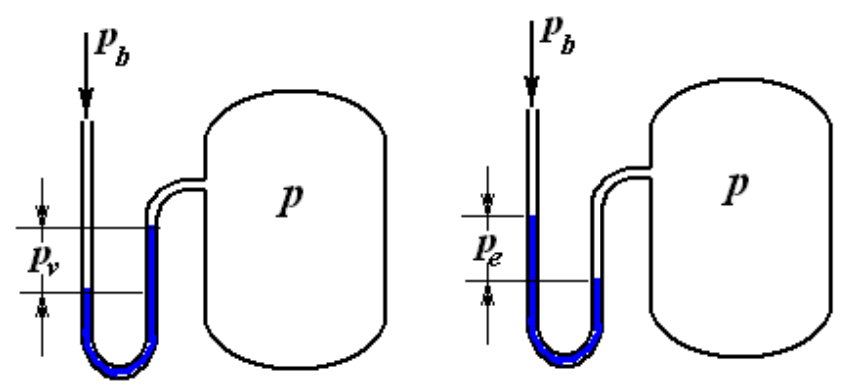
6、比体积和密度
比体积定义为:
密度定义为:
两者互为倒数。
四、平衡状态、状态方程式、坐标图
1、平衡状态
无外界影响,系统保持状态参数不随时间而改变的状态。系统平衡的充要条件是系统同时达到热平衡和力平衡。
热平衡;无外界作用,系统内部、系统与外界处处温度相等。
力平衡:无外界作用,系统内部、系统与外界处处压力相等。
系统平衡时,内部不一定均匀(容器内同时存在气态和液态水);系统稳定时,未必平衡(杆件两端与温度不同的热源接触)。
2、状态方程
状态方程的形式为:
理想气体状态方程的多种形式:
其中
3、状态参数坐标图
简单可压缩系只有两个独立参数,两个变量值可以确定平面坐标上的点,用平面坐标上一点可以确定其状态,任意状态可以在平面坐标上找到对应的点。
五、工质的状态变化过程
1、准平衡过程(准静态状态)
准平衡过程是指偏离平衡态无穷小,随时恢复平衡的状态变化过程。准平衡过程可在状态参数图上用连续实线表示。其进行条件为:破坏平衡的势
2、可逆过程
可逆过程是系统可经原路径恢复至原来状态而在外界不留下任何变化的过程。即可逆同时满足准静态、没有耗散效应。准静态着眼于系统内部平衡,可逆着眼于系统内部及系统与外界作用总效果;一切实际过程均不可逆;可逆过程可用状态参数图上实线表示。
六、过程功和热量
1、功的定义和可逆过程的功
功的热力学定义为:热力系通过边界传递的能量。其计算公式为:
功是过程量,可以使用
IMPORTANT
系统对外做功为正,外界对系统做功为负。
再记不住就跳楼
有用功为
2、热量
热量指仅仅由于温差通过边界传递的能量为热量。
IMPORTANT
系统吸热为正,放热为负。
再记不住就跳楼
可逆过程的热量计算为:
热量是过程量,可以使用
3、热量与功的异同
- 均为通过边界传递的能量;均为过程量;
- 功传递由压力差推动,比体积变化是作功标志;
- 热量传递由温差推动,比熵变化是传热的标志;
- 功是物系间通过宏观运动发生相互作用传递的能量;热是物系间通过紊乱的微粒运动相互作用而传递的能量。
功到热的转化是无条件的;而热到功的转化是有条件、限度的。
七、热力循环
热力循环式封闭的热力过程,在一次循环后,一切状态参数恢复到原值,即
可逆循环是指全部由可逆过程组成的循环。
正向循环(热动力循环)是指输出净功的循环,在
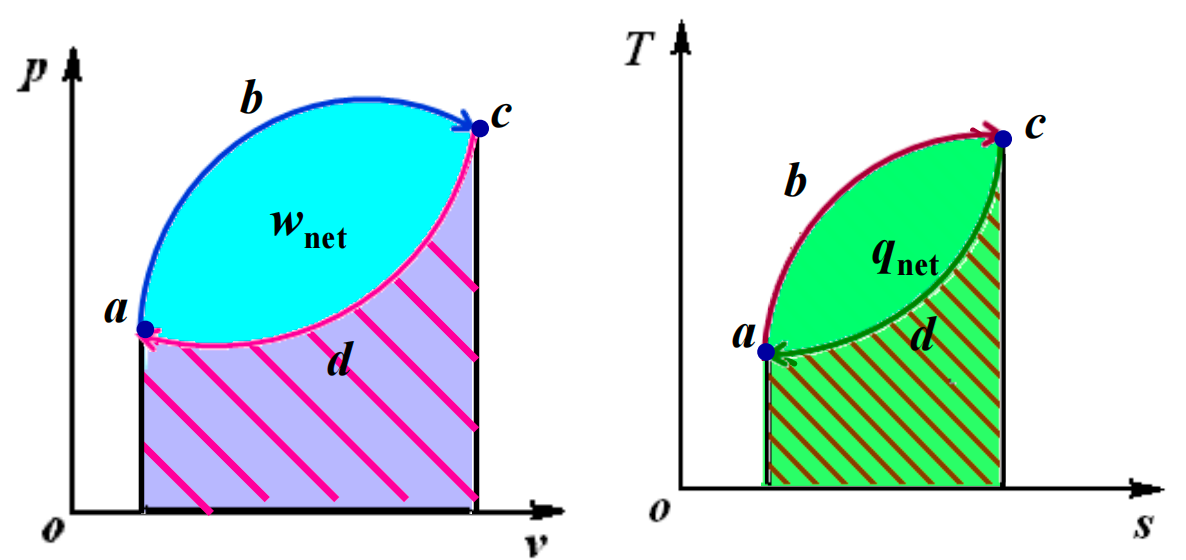
逆向循环指输入净功的循环,在状态参数图中逆时针运行,吸热小于放热。如制冷循环、热泵循环。
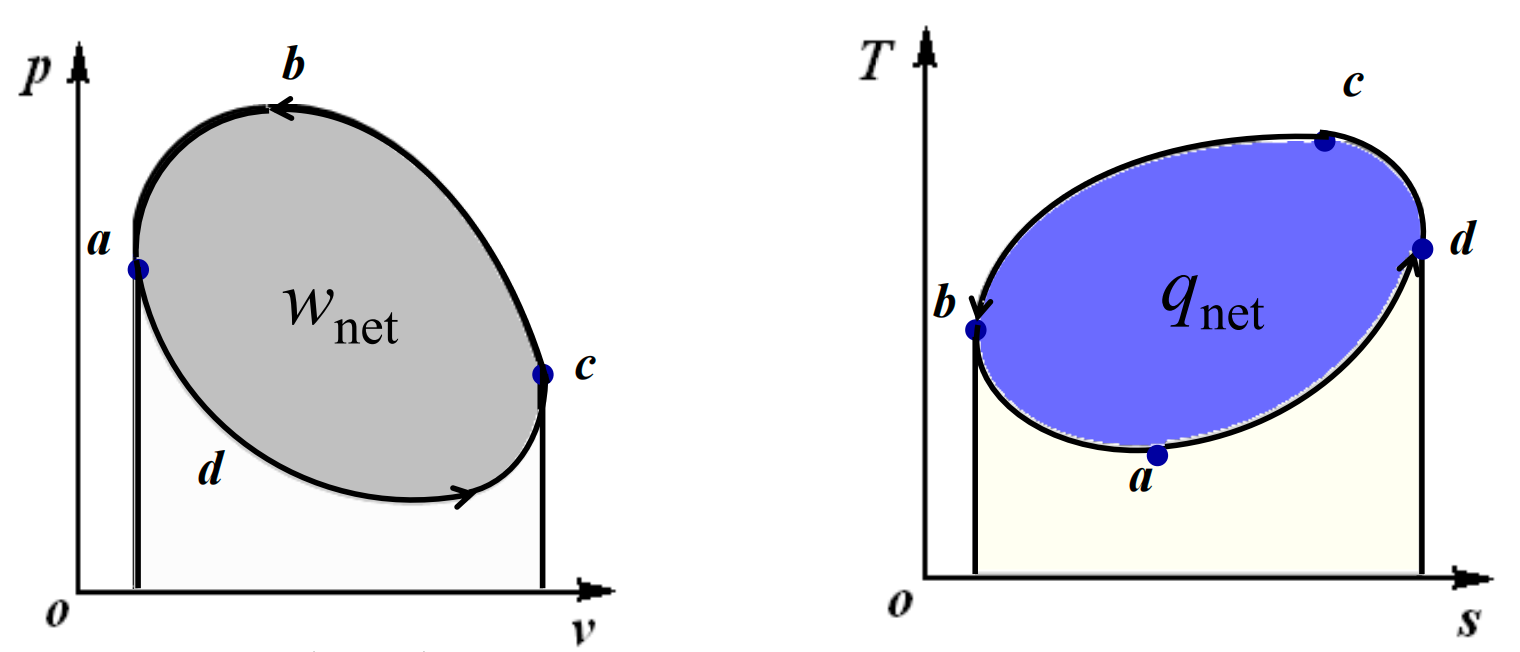
循环经济性指标 收益/代价 来估计,对于正向循环,其热效率为:
逆向循环的制冷系数为:
供热系数为:
